Представляю третью часть цикла постов посвященным ААС, их особенностям и характеристикам. Если вы в первые открыли эту статью, рекомендую обратить внимание на предыдущие:
Продолжим погружаться в эту пучину самых неожиданных вещей, о которых вы, скорее всего, раньше не знали или слышали лишь краем уха. На повестка дня - халотест, или просто хало, самый сильный оральный стероид на рынке. Несмотря на наличие массы подделок на рынке куда часто кладут метилтестостерон вместо хало, дороговизны и редкости, этот препарат пользуется спросом среди атлетов топового уровня и энтузиастов, решающими проверить на собственной шкуре этот препарат.
Халотест явлется мощный андрогенно-анаболическим стероидом, прием которого за короткое время повышает силу и агрессию, так важных в силовых видах спорта.
Рисунок 1.
Халотест (выделен на оси ординат) и слабая (синий цвет) трансактивация глюкокортикойдного рецептора (выделена на оси абсцисс) (48 % по сравнению с дексаметазоном)

Рисунок 2: Антагонизм глюкокортикоидной (ГК) активности .
Халотест оказывает антиглюкокортикоидное действие, слабо связываясь с глюкокортикоидным рецептором в качестве антагониста. Продемонстрировано на рисунках 1 и 2. Поскольку этот конкурентный механизм связывания подтверждается результатами анализов различных тканей (т. е. биоанализа GR CALUX® на млекопитающих и глиальных клеток H-4), он, вероятно, носит системный характер, в отличие от специфичного для скелетных мышц механизма модуляции глюкокортикоидных рецепторов тренболоном.
Антиадопогенный эффект: снижение жировой массы
Экспрессия глюкокортикойдных рецепторов связана с процентом жировой массы и индексом массы тела (ИМТ)
В скелетных мышцах человека наблюдается «умеренная» корреляция (R² = 0,38) между экспрессией глюкокортикойдных рецепторов и процентом жировой массы тела, а также «более значимая» корреляция (R² = 0,70) между экспрессией глюкокортикойдных рецепторов и индексом массы тела (ИМТ), что свидетельствует о взаимодействии между модуляцией глюкокортикоидов флуоксиместероном и регуляцией жировой ткани.
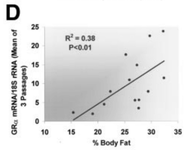
Рисунок 3.
График линейной регрессии, отражающий взаимосвязь между процентом жировой массы тела и GR.
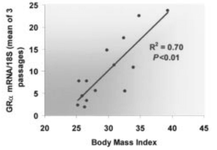
Рисунок 4: График линейной регрессии, отражающий взаимосвязь между ИМТ и глюкокортикоидным рецептором.
Джулиуса А. Вида в книге "Androgens and Anabolic Agents: Chemistry and Pharmacology" пишет:
"Халотестин был разработан в надежде получить значительное увеличение андрогенной и анаболической активности, подобное тому, которое наблюдается в ряду кортикоидов при 9α-фтор-11β-гидрокси-замещении. Было обнаружено, что соединение обладает 9,5-кратной андрогенной и 20-кратной анаболической активностью по сравнению с 17α-метилтестостероном"
Несмотря на то, что флуоксиместерон имеет благоприятное анаболическо-андрогенное соотношение, из-за сильного андрогенного эффекта соединение в основном использовалось как андроген, например, в качестве замены тестостерона при гипогонадизме
ДГТ (5α-дигидротестостерон) является классическим «андрогеном», мощно андрогенным, но лишь слабо анаболическим из-за его интенсивного метаболизма под действием 3α-ГСД [9]. Используемый в качестве исследуемого соединения, ДГТ [сравнимый по своей андрогенной активности с флуоксиместероном] был показан Гуптой, Бхасином и соавторами как способный:
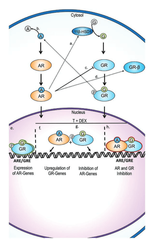
Рисунок 5. Визуализация взаимодействия между андрогенными рецепторами и глюкокортикоидными рецепторами
Заключение
Халотест - бесспорно, один из лучших препаратов для увеличения силовых показателей. Этот препарат отлично подойдет для атлетов силовых видов спорта, особенно когда до помоста остается немного времени. Несмотря на его излишнюю дороговизну и ограниченный доступ, если вы сможете найти настоящий препарат на рынке он даст вам массу профитов. Благодарю за внимание!
Пост основан на статье с сайта thinksteroids.com.
Литература:
[1] Felici, F., Bazzucchi, I., Sgrò, P., Quinzi, F., Conti, A., Aversa, A., … Di Luigi, L. (2016). Acute severe male hypo-testosteronemia affects central motor command in humans. Journal of Electromyography and Kinesiology, 28, 184–192. doi:10.1016/j.jelekin.2015.12.004
[2] Dallek, R. & McGonagle, R. An unfinished life: John F. Kennedy, 1917-1963. Narrated by Richard McGonagle. Time Warner AudioBooks, New York, N.Y., 2003. Audiobook.
[3] Haggerty, D.F., Spector, E.B., Lynch, M., Kern, R., Frank, L.B., & Cederbaum, S.D. (1982). Regulation by Glucocorticoids of Arginase and Argininosuccinate Synthetase in Cultured Rat Hepatoma Cells. J Biol Chem 257, (5). 2246-2253.
[4] Vida, J. Androgens and anabolic agents. Academic Press, Inc. 1969.
[5] Ojasoo, T., Raynaud, J.-P., & Doré, J.-C. (1995). Correspondence factor analysis of steroid libraries. Steroids, 60(6), 458–469. doi:10.1016/0039-128x(95)00005-b
[6] Houtman, C. J., Sterk, S. S., van de Heijning, M. P. M., Brouwer, A., Stephany, R. W., van der Burg, B., & Sonneveld, E. (2009). Detection of anabolic androgenic steroid abuse in doping control using mammalian reporter gene bioassays. Analytica Chimica Acta, 637(1-2), 247–258. doi:10.1016/j.aca.2008.09.037
[7] Whorwood, C. B., Donovan, S. J., Flanagan, D., Phillips, D. I. W., & Byrne, C. D. (2002). Increased Glucocorticoid Receptor Expression in Human Skeletal Muscle Cells May Contribute to the Pathogenesis of the Metabolic Syndrome. Diabetes, 51(4), 1066–1075. doi:10.2337/diabetes.51.4.1066
[8] Fang, H., Tong, W., Branham, W. S., Moland, C. L., Dial, S. L., Hong, H., … Sheehan, D. M. (2003). Study of 202 Natural, Synthetic, and Environmental Chemicals for Binding to the Androgen Receptor. Chemical Research in Toxicology, 16(10), 1338–1358. doi:10.1021/tx030011g
[9] Becker, H., et al. “In vivo uptake and metabolism of 3H-testosterone and 3H-5α-dihydrotestosterone by human benign prostatic hypertrophy.” European Journal of Endocrinology 71.3 (1972): 589-599.
[10] Gupta, V., Bhasin, S., Guo, W., Singh, R., Miki, R., Chauhan, P., … Jasuja, R. (2008). Effects of dihydrotestosterone on differentiation and proliferation of human mesenchymal stem cells and preadipocytes. Molecular and Cellular Endocrinology, 296(1-2), 32–40. doi:10.1016/j.mce.2008.08.019
[11] Furstenberger, C., Vuorinen, A., Da Cunha, T., Kratschmar, D. V., Saugy, M., Schuster, D., & Odermatt, A. (2012). The Anabolic Androgenic Steroid Fluoxymesterone Inhibits 11 -Hydroxysteroid Dehydrogenase 2-Dependent Glucocorticoid Inactivation. Toxicological Sciences, 126(2), 353–361. doi:10.1093/toxsci/kfs022
[12] Barbosa, J., Seal, U. S., & Doe, R. P. (1971). Effects of Anabolic Steroids on Hormone-Binding Proteins, Serum Cortisol and Serum Nonprotein-Bound Cortisol. The Journal of Clinical Endocrinology & Metabolism, 32(2), 232–240. doi:10.1210/jcem-32-2-232
[13] Akalestou, E., Genser, L., & Rutter, G.A. (2020). Glucocorticoid Metabolism in Obesity and Following Weight Loss. Frontiers in Endocrinology, 11. doi: 10.3389/fendo.2020.00059
[14] Spaanderman DCE, Nixon M, Buurstede JC, Sips HC, Schilperoort M, Kuipers EN, Backer EA, Kooijman S, Rensen PCN, Homer NZM, Walker BR, Meijer OC, Kroon J. Androgens modulate glucocorticoid receptor activity in adipose tissue and liver. J Endocrinol. 2018 Oct 1:JOE-18-0503.R1. doi: 10.1530/JOE-18-0503. Epub ahead of print. PMID: 30400038.
[15] Ruiz, D., Padmanabhan, V., & Sargis, P.M. (2020). Stress, sex, and sugar: Glucocorticoids and sex-steroid crosstalk to sex-specific misprogramming of metabolism. Endocrine Society. Aug 2020. 4(8). pp. 1 – 28. doi:10.1210/jendo/bvaa087
Продолжим погружаться в эту пучину самых неожиданных вещей, о которых вы, скорее всего, раньше не знали или слышали лишь краем уха. На повестка дня - халотест, или просто хало, самый сильный оральный стероид на рынке. Несмотря на наличие массы подделок на рынке куда часто кладут метилтестостерон вместо хало, дороговизны и редкости, этот препарат пользуется спросом среди атлетов топового уровня и энтузиастов, решающими проверить на собственной шкуре этот препарат.
Халотест явлется мощный андрогенно-анаболическим стероидом, прием которого за короткое время повышает силу и агрессию, так важных в силовых видах спорта.
Уникальные особенности флуоксиместерона
- Антикатаболические эффекты за счет антагонизма глюкокортикоидного рецептора.
- Антиадипогенные эффекты (снижение жировой массы), вероятно, за счет:
- того же антагонизма глюкокортикоидного рецептора
- андрогенной активности.
Антикатаболический эффект
Флуоксиместерон структурно уникален среди всего спектра коммерчески доступных ААС, поскольку характеризуется наличием α-фтора у C-9 и β-гидроксильной группы у C-11, что придает ему структурное сходство с катаболическими глюкокортикоидами (например, кортизолом, дексаметазоном) [5].Пояснение к антикатаболическому механизму (дополнительно, из предыдущих материалов)
Как указано в более раннем тексте (из первой части серии), эта структурная особенность позволяет флуоксиместерону действовать как антагонист глюкокортикоидного рецептора. В то время как обычные глюкокортикоиды (например, кортизол) связываются с глюкокортикоидным рецептором и запускают катаболизм мышц, халотест занимает тот же рецептор, но не активирует его, блокируя действие кортизола. Это приводит к анти-катаболическому эффекту: мышцы меньше разрушаются под действием стрессовых гормонов.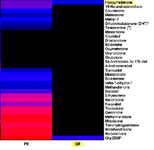
Рисунок 1. Халотест (выделен на оси ординат) и слабая (синий цвет) трансактивация глюкокортикойдного рецептора (выделена на оси абсцисс) (48 % по сравнению с дексаметазоном)

Рисунок 2: Антагонизм глюкокортикоидной (ГК) активности .
Халотест оказывает антиглюкокортикоидное действие, слабо связываясь с глюкокортикоидным рецептором в качестве антагониста. Продемонстрировано на рисунках 1 и 2. Поскольку этот конкурентный механизм связывания подтверждается результатами анализов различных тканей (т. е. биоанализа GR CALUX® на млекопитающих и глиальных клеток H-4), он, вероятно, носит системный характер, в отличие от специфичного для скелетных мышц механизма модуляции глюкокортикоидных рецепторов тренболоном.
Антиадопогенный эффект: снижение жировой массы
Экспрессия глюкокортикойдных рецепторов связана с процентом жировой массы и индексом массы тела (ИМТ)
В скелетных мышцах человека наблюдается «умеренная» корреляция (R² = 0,38) между экспрессией глюкокортикойдных рецепторов и процентом жировой массы тела, а также «более значимая» корреляция (R² = 0,70) между экспрессией глюкокортикойдных рецепторов и индексом массы тела (ИМТ), что свидетельствует о взаимодействии между модуляцией глюкокортикоидов флуоксиместероном и регуляцией жировой ткани.

Рисунок 3.
График линейной регрессии, отражающий взаимосвязь между процентом жировой массы тела и GR.

Рисунок 4: График линейной регрессии, отражающий взаимосвязь между ИМТ и глюкокортикоидным рецептором.
Джулиуса А. Вида в книге "Androgens and Anabolic Agents: Chemistry and Pharmacology" пишет:
"Халотестин был разработан в надежде получить значительное увеличение андрогенной и анаболической активности, подобное тому, которое наблюдается в ряду кортикоидов при 9α-фтор-11β-гидрокси-замещении. Было обнаружено, что соединение обладает 9,5-кратной андрогенной и 20-кратной анаболической активностью по сравнению с 17α-метилтестостероном"
Несмотря на то, что флуоксиместерон имеет благоприятное анаболическо-андрогенное соотношение, из-за сильного андрогенного эффекта соединение в основном использовалось как андроген, например, в качестве замены тестостерона при гипогонадизме
ДГТ (5α-дигидротестостерон) является классическим «андрогеном», мощно андрогенным, но лишь слабо анаболическим из-за его интенсивного метаболизма под действием 3α-ГСД [9]. Используемый в качестве исследуемого соединения, ДГТ [сравнимый по своей андрогенной активности с флуоксиместероном] был показан Гуптой, Бхасином и соавторами как способный:
- Дозозависимо ингибировать накопление липидов [снижать запасание жира]
- Улучшать p-коэффициент (коэффициент эффективности использования питательных веществ) за счет повышения чувствительности к инсулину, чувствительности к лептину и снижения жировой массы
- Направлять преадипоциты (клетки-предшественники) в миогенную (мышечную) линию, а не в адипогенную (жировую), и
- Индуцировать липолиз (расщепление жиров) [10].
Но мы больше не знаем, чем знаем о его антиадипогенных механизмах!
Однако необходимо отметить один момент относительно взаимодействия между модуляцией глюкокортикоидов флуоксиместероном и снижением жировой массы. По аналогии мы можем индуктивно рассуждать, исходя из того, что мы знаем — потому что мы видим своими глазами, — что хвло особенно эффективно снижает жировую массу. Однако мы должны быть осторожны и не втискивать в узкие рамки предположения о кортизоле и жировой массе в случае антагонизма глюкокортикоидных рецепторов со стороны халотеста. Это связано с тем, что:- Халотест также конкурентно ингибирует 11β-ГСД2 [как и оксиметолон с тестостероном], который контролирует окисление кортизола, инактивируя его, тем самым увеличивая эффекты активного кортизола, повышая уровень сывороточного и свободного кортизола [11], [12]. Природа регуляции 11β-ГСД2 в метаболических тканях, включая жировую и скелетные мышцы, не так хорошо изучена по сравнению с его аналогом, 11β-ГСД1, который превращает кортизол в неактивный кортизон [13]. Следовательно, наше понимание того, как этот аспект действия флуоксиместерона влияет на жировые ткани, неполно из-за недостатка литературы.
- Перекрестное взаимодействие между андрогенными рецепторами и глюкокортикоидными рецепторыми в отношении глюкокортикоидов и андрогенов зависит от контекста и ткани [14]. Таким образом, активность флуоксиместерона регулирует транскрипционный выход по-разному в разных метаболических тканях, включая различия между жировыми депо (например, белым или бурым жиром) и скелетными мышцами.
- Природа перекрестного взаимодействия между андрогенными рецепторами и глюкокортикоидных рецепторов плохо определена .

Рисунок 5. Визуализация взаимодействия между андрогенными рецепторами и глюкокортикоидными рецепторами
Заключение
Халотест - бесспорно, один из лучших препаратов для увеличения силовых показателей. Этот препарат отлично подойдет для атлетов силовых видов спорта, особенно когда до помоста остается немного времени. Несмотря на его излишнюю дороговизну и ограниченный доступ, если вы сможете найти настоящий препарат на рынке он даст вам массу профитов. Благодарю за внимание!
Пост основан на статье с сайта thinksteroids.com.
Литература:
[1] Felici, F., Bazzucchi, I., Sgrò, P., Quinzi, F., Conti, A., Aversa, A., … Di Luigi, L. (2016). Acute severe male hypo-testosteronemia affects central motor command in humans. Journal of Electromyography and Kinesiology, 28, 184–192. doi:10.1016/j.jelekin.2015.12.004
[2] Dallek, R. & McGonagle, R. An unfinished life: John F. Kennedy, 1917-1963. Narrated by Richard McGonagle. Time Warner AudioBooks, New York, N.Y., 2003. Audiobook.
[3] Haggerty, D.F., Spector, E.B., Lynch, M., Kern, R., Frank, L.B., & Cederbaum, S.D. (1982). Regulation by Glucocorticoids of Arginase and Argininosuccinate Synthetase in Cultured Rat Hepatoma Cells. J Biol Chem 257, (5). 2246-2253.
[4] Vida, J. Androgens and anabolic agents. Academic Press, Inc. 1969.
[5] Ojasoo, T., Raynaud, J.-P., & Doré, J.-C. (1995). Correspondence factor analysis of steroid libraries. Steroids, 60(6), 458–469. doi:10.1016/0039-128x(95)00005-b
[6] Houtman, C. J., Sterk, S. S., van de Heijning, M. P. M., Brouwer, A., Stephany, R. W., van der Burg, B., & Sonneveld, E. (2009). Detection of anabolic androgenic steroid abuse in doping control using mammalian reporter gene bioassays. Analytica Chimica Acta, 637(1-2), 247–258. doi:10.1016/j.aca.2008.09.037
[7] Whorwood, C. B., Donovan, S. J., Flanagan, D., Phillips, D. I. W., & Byrne, C. D. (2002). Increased Glucocorticoid Receptor Expression in Human Skeletal Muscle Cells May Contribute to the Pathogenesis of the Metabolic Syndrome. Diabetes, 51(4), 1066–1075. doi:10.2337/diabetes.51.4.1066
[8] Fang, H., Tong, W., Branham, W. S., Moland, C. L., Dial, S. L., Hong, H., … Sheehan, D. M. (2003). Study of 202 Natural, Synthetic, and Environmental Chemicals for Binding to the Androgen Receptor. Chemical Research in Toxicology, 16(10), 1338–1358. doi:10.1021/tx030011g
[9] Becker, H., et al. “In vivo uptake and metabolism of 3H-testosterone and 3H-5α-dihydrotestosterone by human benign prostatic hypertrophy.” European Journal of Endocrinology 71.3 (1972): 589-599.
[10] Gupta, V., Bhasin, S., Guo, W., Singh, R., Miki, R., Chauhan, P., … Jasuja, R. (2008). Effects of dihydrotestosterone on differentiation and proliferation of human mesenchymal stem cells and preadipocytes. Molecular and Cellular Endocrinology, 296(1-2), 32–40. doi:10.1016/j.mce.2008.08.019
[11] Furstenberger, C., Vuorinen, A., Da Cunha, T., Kratschmar, D. V., Saugy, M., Schuster, D., & Odermatt, A. (2012). The Anabolic Androgenic Steroid Fluoxymesterone Inhibits 11 -Hydroxysteroid Dehydrogenase 2-Dependent Glucocorticoid Inactivation. Toxicological Sciences, 126(2), 353–361. doi:10.1093/toxsci/kfs022
[12] Barbosa, J., Seal, U. S., & Doe, R. P. (1971). Effects of Anabolic Steroids on Hormone-Binding Proteins, Serum Cortisol and Serum Nonprotein-Bound Cortisol. The Journal of Clinical Endocrinology & Metabolism, 32(2), 232–240. doi:10.1210/jcem-32-2-232
[13] Akalestou, E., Genser, L., & Rutter, G.A. (2020). Glucocorticoid Metabolism in Obesity and Following Weight Loss. Frontiers in Endocrinology, 11. doi: 10.3389/fendo.2020.00059
[14] Spaanderman DCE, Nixon M, Buurstede JC, Sips HC, Schilperoort M, Kuipers EN, Backer EA, Kooijman S, Rensen PCN, Homer NZM, Walker BR, Meijer OC, Kroon J. Androgens modulate glucocorticoid receptor activity in adipose tissue and liver. J Endocrinol. 2018 Oct 1:JOE-18-0503.R1. doi: 10.1530/JOE-18-0503. Epub ahead of print. PMID: 30400038.
[15] Ruiz, D., Padmanabhan, V., & Sargis, P.M. (2020). Stress, sex, and sugar: Glucocorticoids and sex-steroid crosstalk to sex-specific misprogramming of metabolism. Endocrine Society. Aug 2020. 4(8). pp. 1 – 28. doi:10.1210/jendo/bvaa087
