- Сообщения
- 39
- Реакции
- 149
t.me/NR3C4
Продолжаем серию постов посвященным ААС и их свойствам для наших бравых пользователей. В прошлом посте мы рассмотрели тренболон (нажми на ссылку, чтобы прочитать). Теперь же мы рассмотри станазолол, или в простонародье: стан, винни и прочее-прочее.
Станозолол является представителем гетероциклических ААС, что характеризуется присоединением пиразольного кольца к его А-кольцу. Помимо продления продолжительности биологических эффектов («периода полувыведения»), эта химическая модификация стероидного ядра оказывает и другие эффекты, которые подразумевают интересные изменения, уникальные для этого препарата:
Хотя станозолол имеет тенденцию снижать абсолютный уровень ИФР-І, его применение в сочетании с ароматизирующимся андрогеном и гормоном роста, которые оба значительно повышают его, увеличивает свободную, активную фракцию ИФР-І за счет снижения уровня ИФРСБ-3.
Инсулиноподобный фактор роста 1 (ИФР-І) является мощным фактором роста, связанным с общим размером тела. ИФР-І индуцирует митоз — деление клеток — увеличивая количество клеток в тканях организма. Таким образом, ИФР-І является митогенным — он стимулирует деление клеток, чтобы "выращивать всё". В клетках скелетных мышц человека миогенез — это процесс, в ходе которого новые мышечные волокна возникают в результате слияния примордиальных мышечных волокон, называемых миобластами (т.е. гиперплазия скелетных мышц; механизмы гипертрофии скелетных мышц человека, зависящие от слияния клеток). Во время миогенеза (восстановления мышц) миобласты сливаются вместе, образуя многоядерные миотрубки, которые в конечном итоге созревают в полноценно функционирующие мышечные волокна.
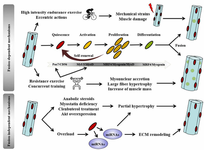
Механизмы гипертрофии скелетных мышц человека, зависящие от слияния сателлитных клеток, и механизмы, не зависящие от него
Самые используемые ААС также индуцирует механизмы гипертрофии (ремоделирования мышц), независимые от слияния клеток, посредством процессов увеличения синтеза белка и снижения катаболизма белка, увеличивая площадь поперечного сечения существующих мышечных волокон за счет добавления существующих миоядер.
В кровотоке ИФР-І связан с различными ИФРСБ, особенно с крупным ИФРСБ-3 и его ассоциированной кислото-лабильной субъединицей (КЛС), что уменьшает биодоступность ИФР-І, но продлевает его период полувыведения в кровотоке. Связывание ИФР-І с КЛС предотвращает транспорт через сосудистый компартмент — по сути, поддерживая уровень ИФР-І в сыворотке повышенным, потому что он не может покинуть кровь. И наоборот, связывание ИФР-І с более мелкими белками (ИФРСБ-1, ИФРСБ-2 и ИФРСБ-6) может облегчать проникновение в ткани.
Около 70% системного ИФР-І циркулирует в виде ~150 кДа тройного (или третичного) комплекса, состоящего из ИФР-І + ИФРСБ-3 + КЛС.
Около 20–25% системного ИФР-І находится в виде более мелкого (~39–44 кДа) бинарного комплекса, состоящего из ИФР-І + ИФРСБ-3, который может пересекать сосудистую границу и может оказывать эффекты на конечные органы.
Менее 10% системного ИФР-І находится в 7,5 кДа свободной активной форме (период полувыведения 12 минут).
В клетках скелетных мышц человека ИФРСБ-3 особенно много, и волокна дополнительно насыщены -СБ-2 (считается малым ингибирующим белком) и более низкими уровнями -СБ-4 и -СБ-5.
К сожалению, здравый подход к стимуляции секреции ИФР-І печенью путем введения ГР представляет собой проблему: поскольку ГР является основным стимулятором ИФРСБ-3 и КЛС, экзогенный супрафизиологический ГР увеличивает общую фракцию свободного ИФР-І, одновременно снижая его относительную биоактивность, по аналогии со свободным тестостероном в сравнении с супрафизиологическим тестостероном (через увеличение альбумина), свободными андрогенами (не связанными с гспг) и ААС.
Исходя из вышеперечисленного можно предположить, что станазолол может гипотетически подходить как препарат для увеличения биодоступности ИФР1 по отношению к ГР, подобно провирону по отношению к ААС. Но если эффект последнего на ГСПГ довольно слаб по сравнению с собственно андрогенным эффектом на него (т.е. чтобы значительно снизить его), то станозолол, вероятно, будет лучше в сравнении для практического применения.
В печени LAGS представляет собой сайт связывания глюкокортикоидов, таких как кортизол, с низким сродством, который слабо связывает свободные циркулирующие катаболические гормоны. Только для станозолола было продемонстрировано, что он вызывает время- и дозозависимую инактивацию сайта связывания LAGS, которая была необратимой, что предполагает отрицательную аллостерическую модуляцию связывания глюкокортикоидов с LAGS.
Станозолол наиболее эффективен среди 17ААС (станозолол > флуоксиместерон > метандиенон > метилтестостерон) в отношении:
Эта уникальная особенность станозолола, следовательно, неблагоприятна. = усиленный мышечный катаболизм (не есть хорошо™).
Станозолол является замечательно эффективным ингибитором PR, проявляя ½ своей эффективности при низкой концентрации 0,1188 мкМ.
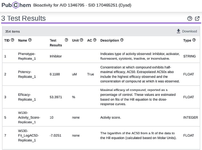
Результаты тестирования в PubChem на биологическую активность (ингибирование) в отношении рецептора прогестерона.
Как и эта модификация по C-17, модификация, сделанная у станозолола — добавление пиразольного кольца, конденсированного с соединением между вторым и третьим атомами углерода кольца А 5α-дигидростеранового кольца — служит для еще большего продления анаболического эффекта за счет печеночного метаболизма. 3 до 7 ч в зависимости от источника авторитетных данных (т.е. Hazardous Substances Data Bank против DrugBank), странно точный 9,2 ч биологический период полувыведения флуоксиместерона объясняет его обычные рекомендации по назначению для взрослых для использования в дозе от 10 до 40 мг ежедневно в 1–4 приемах, т.е. каждые 4 часа), и даже принимая неприменимые данные для внутривенного (в/в) введения для туринабола, показывающие его 16-часовой терминальный период полувыведения (парентеральное введение продлевает биоактивность), биологический период полувыведения станозолола > 24 ч поразителен, поскольку он на 50% больше, чем терминальный период полувыведения ОТ после внутривенной инфузии.
Часовые биологические периоды полувыведения 17ААС значительно длиннее, чем у принятой внутрь (перорально, проглатывание) базового гормона. Например, выпивание флакона тестостерона, предназначенного для инъекций, не даст вам ничего с точки зрения результатов из-за его быстрого метаболизма и выведения; и это не будет особенно токсичным (хотя очевидно такое лучше не делать ). Медицинская гипотеза, опубликованная в одноименном журнале докторами Питером Бондом, Уильямом Ллевеллином и Питером Ван Молом, представляет убедительный аргумент о гепатотоксичности 17ААС как функции активации АР, ведущей к увеличению активных форм кислорода (ROS) через β-окисление митохондриальных жирных кислот в клетках печени, т.е. гепатотоксичность ≈ потенциал трансактивацииАР × t1/21/2/(kee * Vdd) доза (мг), или, говоря более просто, – гепатотоксичность препарата является произведением его анаболической активности и устойчивости к печеночному распаду.
). Медицинская гипотеза, опубликованная в одноименном журнале докторами Питером Бондом, Уильямом Ллевеллином и Питером Ван Молом, представляет убедительный аргумент о гепатотоксичности 17ААС как функции активации АР, ведущей к увеличению активных форм кислорода (ROS) через β-окисление митохондриальных жирных кислот в клетках печени, т.е. гепатотоксичность ≈ потенциал трансактивацииАР × t1/21/2/(kee * Vdd) доза (мг), или, говоря более просто, – гепатотоксичность препарата является произведением его анаболической активности и устойчивости к печеночному распаду.
Для нормального (т.е. здорового) взрослого юзера станозолола это повышенное содержание C1-ИНГ, вероятно, снижает C1-ИНГдо субнормального уровня, тем самым уменьшая проницаемость сосудов, что, в свою очередь, снижает доставку жидкости и питательных веществ к суставам, необходимых для здорового функционирования.
Итоги
Станазалол является отличным препаратом для сушки. Сочетание с гормоном роста имеет вес, поскольку он увеличивает свободную фракцию ИФР-1. Его гепатотоксичность требует воздержание от приема алкоголя, чрезмерно жирной пищи и ряда других веществ, крайне негативно сказывающихся на работу в печени. Впрочем, все мы знаем, что гептрал и УДХК всему голова . Наконец, внимательно следите за суставами на курсе станазолола - возможно где-то все таки стоит намотать бинты и взять пояс со страховкой, если у вас высокие дозировки стана, большая длительность приема или иные факторы, усугубляющие состояние коллагеновых структур на курсе, лучше подстраховаться.
. Наконец, внимательно следите за суставами на курсе станазолола - возможно где-то все таки стоит намотать бинты и взять пояс со страховкой, если у вас высокие дозировки стана, большая длительность приема или иные факторы, усугубляющие состояние коллагеновых структур на курсе, лучше подстраховаться.
Пост основан на статье с сайта thinksteroids.com.
Литература:
[1] Fryburg, D. A., Weltman, A., Jahn, L. A., Weltman, J.Y., Samojlik, E., Hintz, R. L., & Veldhuis, J. D. (1997). Short-Term Modulation of the Androgen Milieu Alters Pulsatile, But Not Exercise- or Growth Hormone (GH)-Releasing Hormone-Stimulated GH Secretion in Healthy Men: Impact of Gonadal Steroid and GH Secretory Changes on Metabolic Outcomes1. The Journal of Clinical Endocrinology & Metabolism, 82(11), 3710–3719. do i:10.1210/jcem.82.11.4379
[2] Betancor-Hernández, E., Pérez-Machı́n, R., Henrı́quez-Hernández, L., Mateos-Dı́az, C., Novoa-Mogollón, J., & Fernández-Pérez, L. (2003). Photoaffinity labeling identification of thyroid hormone-regulated glucocorticoi d-binding peptides in rat liver endoplasmic reticulum: an oligomeric protein with high affinity for 16β-hydroxylated stanozolol. The Journal of Steroid Biochemistry and Molecular Biology, 87(4-5), 253–264. doi:10.1016/j.jsbmb.2003.09.009
[3] National Center for Biotechnology Information. “PubChem Bioassay Record for Bioactivity AID 1346795 – SID 170465251, Source: Tox21” PubChem, pubchem.ncbi.nlm.nih.gov/bioassay/1346795#sid=170465251. Accessed 23 June, 2024.
[4] DrugBank 6.0: the DrugBank Knowledgebase for 2024. “Stanozolol, Record: DB06718” DrugBank, drugbank.ca/drugs/DB06718. Accessed 23 June, 2024.
[5] Ellis AJ, Cawston TE, Mackie EJ. The differential effects of stanozolol on human skin and synovial fibroblasts in vitro: DNA synthesis and receptor binding. Agents Actions. 1994 Mar;41(1-2):37-43. doi: 10.1007/BF01986391
[6] Sloane, D. E., Lee, C. W., & Sheffer, A. L. (2007). Hereditary angioedema: Safety of long-term stanozolol therapy. Journal of Allergy and Clinical Immunology, 120(3), 654–658. doi:10.1016/j.jaci.2007.06.037
[7] Cugno, M., Zanichelli, A., Foieni, F., Caccia, S., & Cicardi, M. (2009). C1-inhibitor deficiency and angioedema: molecular mechanisms and clinical progress. Trends in Molecular Medicine, 15(2), 69–78. doi:10.1016/j.molmed.2008.12.001
[8] Solsona R, Pavlin L, Bernardi H, Sanchez AM. Molecular Regulation of Skeletal Muscle Growth and Organelle Biosynthesis: Practical Recommendations for Exercise Training. (2021). Int J Mol Sci. 22(5):2741. doi: 10.3390/ijms22052741
[9] Foulstone, E. J., Savage, P. B., Crown, A. L., Holly, J. M. P., & Stewart, C. E. H. (2003). Role of insulin-like growth factor binding protein-3 (IGFBP-3) in the differentiation of primary human adult skeletal myoblasts. Journal of Cellular Physiology, 195(1), 70–79. doi:10.1002/jcp.10227
[10] Hadley JS, Hinds CJ. Anabolic strategies in critical illness. Curr Opin Pharmacol. 2002 Dec;2(6):700-7. doi:10.1016/s1471-4892(02)00217-5
[11] Kelley, K. M., Oh, Y., Gargosky, S. E., Gucev, Z., Matsumoto, T., Hwa, V., … Rosenfeld, R. G. (1996). Insulin-like growth factor-binding proteins (IGFBPs) and their regulatory dynamics. The International Journal of Biochemistry & Cell Biology, 28(6), 619–637. doi:10.1016/1357-2725(96)00005-2
[12] Guler, H.-P., Zapf, J., Schmid, C., & Froesch, E. R. (1989). Insulin-like growth factors I and II in healthy man. European Journal of Endocrinology, 121(6), 753–758. doi:10.1530/acta.0.1210753
[13] Fernández, L., Chirino, R., Boada, L. D., Navarro, D., Cabrera, N., del Rio, I., & Díaz-Chico, B. N. (1994). Stanozolol and danazol, unlike natural androgens, interact with the low affinity glucocorticoid-binding sites from male rat liver microsomes. Endocrinology, 134(3), 1401–1408. doi:10.1210/endo.134.3.8119180
[14] Betancor-Hernández, E., Pérez-Machı́n, R., Henrı́quez-Hernández, L., Mateos-Dı́az, C., Novoa-Mogollón, J., & Fernández-Pérez, L. (2003). Photoaffinity labeling identification of thyroid hormone-regulated glucocorticoid-binding peptides in rat liver endoplasmic reticulum: an oligomeric protein with high affinity for 16β-hydroxylated stanozolol. The Journal of Steroid Biochemistry and Molecular Biology, 87(4-5), 253–264. doi:10.1016/j.jsbmb.2003.09.009
[15] Bond P, Llewellyn W, Van Mol P. Anabolic androgenic steroid-induced hepatotoxicity. Med Hypotheses. 2016 Aug;93:150-3. doi: 10.1016/j.mehy.2016.06.004
[16] Sloane, D. E., Lee, C. W., & Sheffer, A. L. (2007). Hereditary angioedema: Safety of long-term stanozolol therapy. Journal of Allergy and Clinical Immunology, 120(3), 654–658. doi:10.1016/j.jaci.2007.06.037
[17] P. Niravath, Aromatase inhibitor-induced arthralgia: a review, Annals of Oncology, Volume 24, Issue 6, 2013, Pages 1443-1449, ISSN 0923-7534, doi.org/10.1093/annonc/mdt037.
Продолжаем серию постов посвященным ААС и их свойствам для наших бравых пользователей. В прошлом посте мы рассмотрели тренболон (нажми на ссылку, чтобы прочитать). Теперь же мы рассмотри станазолол, или в простонародье: стан, винни и прочее-прочее.
Станозолол является представителем гетероциклических ААС, что характеризуется присоединением пиразольного кольца к его А-кольцу. Помимо продления продолжительности биологических эффектов («периода полувыведения»), эта химическая модификация стероидного ядра оказывает и другие эффекты, которые подразумевают интересные изменения, уникальные для этого препарата:
Уникальные особенности станозолола
- Митогенные (клеточное деление непосредственно) и миогенные (связзанные с ответной реакцией на растяжение) эффекты за счет вероятного увеличения биодоступности свободного ИФР-І путем снижения ИФРСБ-3 [1].
- Модуляция глюкокортикоидов путем прямого и опосредованного (через его 16β-гидроксилированный метаболит 16β-СТ) отрицательного регулирования сайта связывания глюкокортикоидов с низкой аффинностью (в английском исполнение LAGS, далее так и будем именовать) в печени.
- Антипрогестагенные эффекты за счет антагонизма PR (рецептора прогестерона).
- Чрезвычайно длительная биологическая активность («период полувыведения») > 24 часов, что примечательно среди 17α-алкилированных ААС.
- Боль в суставах: станозолол, печально известный связью с болью в суставах («ноющие, сухие суставы»), воздействует на синовиальные фибробласты — предшественники клеток, составляющих синовиальные суставы (например, тазобедренные, коленные, плечевые), подавляя синтез ДНК и, возможно, вторично за счет (особенно сильной) стимуляции активности С1-ингибитора (C1-ИНГ) — что не уникально для станозолола, но характерно для 17ААС, — что, вероятно, снижает проницаемость сосудов и влияет на смазку суставов и доставку питательных веществ к суставам.
Митогенные и миогенные эффекты
Станозолол снижает уровень инсулиноподобного фактора роста, связывающего белок 3 (ИФРСБ-3), тем самым, вероятно, увеличивая биодоступность ИФР-І (свободный ИФР-І)Хотя станозолол имеет тенденцию снижать абсолютный уровень ИФР-І, его применение в сочетании с ароматизирующимся андрогеном и гормоном роста, которые оба значительно повышают его, увеличивает свободную, активную фракцию ИФР-І за счет снижения уровня ИФРСБ-3.
Инсулиноподобный фактор роста 1 (ИФР-І) является мощным фактором роста, связанным с общим размером тела. ИФР-І индуцирует митоз — деление клеток — увеличивая количество клеток в тканях организма. Таким образом, ИФР-І является митогенным — он стимулирует деление клеток, чтобы "выращивать всё". В клетках скелетных мышц человека миогенез — это процесс, в ходе которого новые мышечные волокна возникают в результате слияния примордиальных мышечных волокон, называемых миобластами (т.е. гиперплазия скелетных мышц; механизмы гипертрофии скелетных мышц человека, зависящие от слияния клеток). Во время миогенеза (восстановления мышц) миобласты сливаются вместе, образуя многоядерные миотрубки, которые в конечном итоге созревают в полноценно функционирующие мышечные волокна.

Механизмы гипертрофии скелетных мышц человека, зависящие от слияния сателлитных клеток, и механизмы, не зависящие от него
Самые используемые ААС также индуцирует механизмы гипертрофии (ремоделирования мышц), независимые от слияния клеток, посредством процессов увеличения синтеза белка и снижения катаболизма белка, увеличивая площадь поперечного сечения существующих мышечных волокон за счет добавления существующих миоядер.
ИФРСБ: Фокус на ИФРСБ-3 в отношении ИФР-І
У человека существует шесть ИФРСБ, которые по-разному модулируют активность ИФР-І, продлевая период полувыведения ИФР-І и либо потенцируя, либо ингибируя связывание ИФР-І с его рецептором (ИФР-1R).В кровотоке ИФР-І связан с различными ИФРСБ, особенно с крупным ИФРСБ-3 и его ассоциированной кислото-лабильной субъединицей (КЛС), что уменьшает биодоступность ИФР-І, но продлевает его период полувыведения в кровотоке. Связывание ИФР-І с КЛС предотвращает транспорт через сосудистый компартмент — по сути, поддерживая уровень ИФР-І в сыворотке повышенным, потому что он не может покинуть кровь. И наоборот, связывание ИФР-І с более мелкими белками (ИФРСБ-1, ИФРСБ-2 и ИФРСБ-6) может облегчать проникновение в ткани.
Около 70% системного ИФР-І циркулирует в виде ~150 кДа тройного (или третичного) комплекса, состоящего из ИФР-І + ИФРСБ-3 + КЛС.
Около 20–25% системного ИФР-І находится в виде более мелкого (~39–44 кДа) бинарного комплекса, состоящего из ИФР-І + ИФРСБ-3, который может пересекать сосудистую границу и может оказывать эффекты на конечные органы.
Менее 10% системного ИФР-І находится в 7,5 кДа свободной активной форме (период полувыведения 12 минут).
В клетках скелетных мышц человека ИФРСБ-3 особенно много, и волокна дополнительно насыщены -СБ-2 (считается малым ингибирующим белком) и более низкими уровнями -СБ-4 и -СБ-5.
Практическое применение
Из 10 мг среднесуточной выработки ИФР-І у здорового нормального мужчины («эндогенные уровни»), примерно 1 мг (т.е. свободная фракция за 24-часовой цикл кровообращения) оказывает системный биологический эффект, который мы больше всего желаем в соответствии с гипотезой свободного гормона.К сожалению, здравый подход к стимуляции секреции ИФР-І печенью путем введения ГР представляет собой проблему: поскольку ГР является основным стимулятором ИФРСБ-3 и КЛС, экзогенный супрафизиологический ГР увеличивает общую фракцию свободного ИФР-І, одновременно снижая его относительную биоактивность, по аналогии со свободным тестостероном в сравнении с супрафизиологическим тестостероном (через увеличение альбумина), свободными андрогенами (не связанными с гспг) и ААС.
Исходя из вышеперечисленного можно предположить, что станазолол может гипотетически подходить как препарат для увеличения биодоступности ИФР1 по отношению к ГР, подобно провирону по отношению к ААС. Но если эффект последнего на ГСПГ довольно слаб по сравнению с собственно андрогенным эффектом на него (т.е. чтобы значительно снизить его), то станозолол, вероятно, будет лучше в сравнении для практического применения.
Модуляция глюкокортикоидов
Станозолол отрицательно регулирует сайт связывания глюкокортикоидов с низким сродством (LAGS)В печени LAGS представляет собой сайт связывания глюкокортикоидов, таких как кортизол, с низким сродством, который слабо связывает свободные циркулирующие катаболические гормоны. Только для станозолола было продемонстрировано, что он вызывает время- и дозозависимую инактивацию сайта связывания LAGS, которая была необратимой, что предполагает отрицательную аллостерическую модуляцию связывания глюкокортикоидов с LAGS.
Станозолол наиболее эффективен среди 17ААС (станозолол > флуоксиместерон > метандиенон > метилтестостерон) в отношении:
- ↓ сродства глюкокортикоидов (например, кортизола)
- ↓ количества сайтов связывания LAGS
- ↑ скорости диссоциации глюкокортикоидов от сайтов связывания глюкокортикоидов [13].
Практическое применение
Но вот в чем «загвоздка» — чистым системным следствием этой отрицательной регуляции станозололом является эффективное увеличение классического ГР-сигналинга (т.е. усиление катаболизма скелетных мышц) за счет увеличения доступности глюкокортикоидов для цитозольного ГР.Эта уникальная особенность станозолола, следовательно, неблагоприятна. = усиленный мышечный катаболизм (не есть хорошо™).
Антипрогестагенные эффекты
Станозолол антагонизирует рецептор прогестерона (PR)Станозолол является замечательно эффективным ингибитором PR, проявляя ½ своей эффективности при низкой концентрации 0,1188 мкМ.

Результаты тестирования в PubChem на биологическую активность (ингибирование) в отношении рецептора прогестерона.
Токсичность, а также продолжительность биологических эффектов
Станозолол имеет удивительно длительный > 24 часа биологический период полувыведенияОпределения и понятия
- Биологический период полувыведения: концепция однодозовой фармакокинетики, мера времени (ч, мин, сек), описывающая продолжительность, в течение которой препарат остается активным в организме после приема (т.е. перорально, проглатывание) или парентерального введения (например, внутримышечно, внутривенно). Он измеряется как время, в течение которого концентрация препарата снижается до ½ исходной концентрации, и отражает метаболизм и/или выведение.
- Терминальный период полувыведения: концепция многодозовой фармакокинетики, мера времени (ч, мин, сек), описывающая продолжительность, в течение которой препарат остается активным в организме после прекращения всего дозирования (т.е. после «курса» или «цикла»). Это измерение того, как долго препарат остается, даже в неактивной форме, в организме после прекращения всего дозирования, и в нашем случае (в случае инъекций этерифицированных ААС, предназначенных для повышения уровня в крови до равновесия в течение нескольких недель) он намного длиннее, чем биологический период полувыведения препарата.
Контекстуализация данных
Препараты 17ААС (17α-алкилированные; например, станозолол, метандиенон, оксиметолон) характеризуются относительно длительным периодом полувыведения из-за добавления метильной группы в α-ориентированной плоскости 17-го углерода классического стероидного ядра или стеранового кольца. Это 17α-алкилирование способствует продлению анаболического эффекта за счет печеночного метаболизма и ингибирует ароматизацию А-кольца в эстрогены.Как и эта модификация по C-17, модификация, сделанная у станозолола — добавление пиразольного кольца, конденсированного с соединением между вторым и третьим атомами углерода кольца А 5α-дигидростеранового кольца — служит для еще большего продления анаболического эффекта за счет печеночного метаболизма. 3 до 7 ч в зависимости от источника авторитетных данных (т.е. Hazardous Substances Data Bank против DrugBank), странно точный 9,2 ч биологический период полувыведения флуоксиместерона объясняет его обычные рекомендации по назначению для взрослых для использования в дозе от 10 до 40 мг ежедневно в 1–4 приемах, т.е. каждые 4 часа), и даже принимая неприменимые данные для внутривенного (в/в) введения для туринабола, показывающие его 16-часовой терминальный период полувыведения (парентеральное введение продлевает биоактивность), биологический период полувыведения станозолола > 24 ч поразителен, поскольку он на 50% больше, чем терминальный период полувыведения ОТ после внутривенной инфузии.
Часовые биологические периоды полувыведения 17ААС значительно длиннее, чем у принятой внутрь (перорально, проглатывание) базового гормона. Например, выпивание флакона тестостерона, предназначенного для инъекций, не даст вам ничего с точки зрения результатов из-за его быстрого метаболизма и выведения; и это не будет особенно токсичным (хотя очевидно такое лучше не делать
Боль в суставах
Ингибирование синтеза ДНК в синовиальных клетках
Станозолол ингибирует синтез ДНК в синовиальных клетках, которые составляют хрящ крупных суставов, таких как тазобедренные, коленные и плечевые. Ингибирование синтеза ДНК приводит к замедлению скорости и способности регенерации тканей. Поскольку эти ткани уже характеризуются относительно медленной скоростью восстановления — отсюда необходимость хирургического вмешательства при катастрофических травмах — по сравнению со скелетными мышцами, это приводит к более хрупким, менее прочным сухожилиям в крупных суставах при использовании станозолола.Повышенная активность C1-ИНГснижает проницаемость сосудов, что может уменьшить смазку суставов и доставку питательных веществ к суставам
Эффективность станозолола в повышении активности С1-ингибитора (C1-ИНГ) является причиной его эффективности при лечении наследственного ангиоотека (HAE) — состояния, характеризующегося отеком слизистых оболочек, из-за которого пациенты страдают от переполнения тканей жидкостью. C1-ИНГ является многосериевым ингибитором протеазы, который контролирует несколько каталитических путей, включая активацию классического компонента. HAE возникает из-за ↓ C1-ИНГ. C1-ИНГ подавляет брадикинин, который через действие на B₂R опосредует вазодилатацию и усиливает проницаемость, что приводит к ангиоотеку [7]. Когда C1-ИНГ снижен, возникает ↑ проницаемости сосудов (подкожная и подслизистая) — вызывая ангиоотек — из-за ↑ брадикинина (который C1-ИНГ ослабляет) [из-за воздействия на классическую контактную систему и активацию комплемента]. Станозолол повышает экспрессию гена C1-ИНГ и активность плазменной аминопептидазы P (катаболизирует кинины). Станозолол, вероятно, усиливает выработку C1-ИНГ в печени прямым действием на печень, а не действием через андрогенные рецепторы сам по себе.Для нормального (т.е. здорового) взрослого юзера станозолола это повышенное содержание C1-ИНГ, вероятно, снижает C1-ИНГдо субнормального уровня, тем самым уменьшая проницаемость сосудов, что, в свою очередь, снижает доставку жидкости и питательных веществ к суставам, необходимых для здорового функционирования.
Практическое применение
Обматывание суставов при выполнении тяжелых упражнений во время тренировок с отягощениями является разумным во время курса станозолола. Поскольку ингибиторы ароматазы (ИА) имеют тенденцию вызывать артралгию (боль в суставах), увеличивая выработку провоспалительных цитокинов в синовиальных клетках этих суставов, возможно, разумно корректировать дозу и выбор ИА в зависимости от симптоматики и переносимости станозолола.Итоги
Станазалол является отличным препаратом для сушки. Сочетание с гормоном роста имеет вес, поскольку он увеличивает свободную фракцию ИФР-1. Его гепатотоксичность требует воздержание от приема алкоголя, чрезмерно жирной пищи и ряда других веществ, крайне негативно сказывающихся на работу в печени. Впрочем, все мы знаем, что гептрал и УДХК всему голова
Пост основан на статье с сайта thinksteroids.com.
Литература:
[1] Fryburg, D. A., Weltman, A., Jahn, L. A., Weltman, J.Y., Samojlik, E., Hintz, R. L., & Veldhuis, J. D. (1997). Short-Term Modulation of the Androgen Milieu Alters Pulsatile, But Not Exercise- or Growth Hormone (GH)-Releasing Hormone-Stimulated GH Secretion in Healthy Men: Impact of Gonadal Steroid and GH Secretory Changes on Metabolic Outcomes1. The Journal of Clinical Endocrinology & Metabolism, 82(11), 3710–3719. do i:10.1210/jcem.82.11.4379
[2] Betancor-Hernández, E., Pérez-Machı́n, R., Henrı́quez-Hernández, L., Mateos-Dı́az, C., Novoa-Mogollón, J., & Fernández-Pérez, L. (2003). Photoaffinity labeling identification of thyroid hormone-regulated glucocorticoi d-binding peptides in rat liver endoplasmic reticulum: an oligomeric protein with high affinity for 16β-hydroxylated stanozolol. The Journal of Steroid Biochemistry and Molecular Biology, 87(4-5), 253–264. doi:10.1016/j.jsbmb.2003.09.009
[3] National Center for Biotechnology Information. “PubChem Bioassay Record for Bioactivity AID 1346795 – SID 170465251, Source: Tox21” PubChem, pubchem.ncbi.nlm.nih.gov/bioassay/1346795#sid=170465251. Accessed 23 June, 2024.
[4] DrugBank 6.0: the DrugBank Knowledgebase for 2024. “Stanozolol, Record: DB06718” DrugBank, drugbank.ca/drugs/DB06718. Accessed 23 June, 2024.
[5] Ellis AJ, Cawston TE, Mackie EJ. The differential effects of stanozolol on human skin and synovial fibroblasts in vitro: DNA synthesis and receptor binding. Agents Actions. 1994 Mar;41(1-2):37-43. doi: 10.1007/BF01986391
[6] Sloane, D. E., Lee, C. W., & Sheffer, A. L. (2007). Hereditary angioedema: Safety of long-term stanozolol therapy. Journal of Allergy and Clinical Immunology, 120(3), 654–658. doi:10.1016/j.jaci.2007.06.037
[7] Cugno, M., Zanichelli, A., Foieni, F., Caccia, S., & Cicardi, M. (2009). C1-inhibitor deficiency and angioedema: molecular mechanisms and clinical progress. Trends in Molecular Medicine, 15(2), 69–78. doi:10.1016/j.molmed.2008.12.001
[8] Solsona R, Pavlin L, Bernardi H, Sanchez AM. Molecular Regulation of Skeletal Muscle Growth and Organelle Biosynthesis: Practical Recommendations for Exercise Training. (2021). Int J Mol Sci. 22(5):2741. doi: 10.3390/ijms22052741
[9] Foulstone, E. J., Savage, P. B., Crown, A. L., Holly, J. M. P., & Stewart, C. E. H. (2003). Role of insulin-like growth factor binding protein-3 (IGFBP-3) in the differentiation of primary human adult skeletal myoblasts. Journal of Cellular Physiology, 195(1), 70–79. doi:10.1002/jcp.10227
[10] Hadley JS, Hinds CJ. Anabolic strategies in critical illness. Curr Opin Pharmacol. 2002 Dec;2(6):700-7. doi:10.1016/s1471-4892(02)00217-5
[11] Kelley, K. M., Oh, Y., Gargosky, S. E., Gucev, Z., Matsumoto, T., Hwa, V., … Rosenfeld, R. G. (1996). Insulin-like growth factor-binding proteins (IGFBPs) and their regulatory dynamics. The International Journal of Biochemistry & Cell Biology, 28(6), 619–637. doi:10.1016/1357-2725(96)00005-2
[12] Guler, H.-P., Zapf, J., Schmid, C., & Froesch, E. R. (1989). Insulin-like growth factors I and II in healthy man. European Journal of Endocrinology, 121(6), 753–758. doi:10.1530/acta.0.1210753
[13] Fernández, L., Chirino, R., Boada, L. D., Navarro, D., Cabrera, N., del Rio, I., & Díaz-Chico, B. N. (1994). Stanozolol and danazol, unlike natural androgens, interact with the low affinity glucocorticoid-binding sites from male rat liver microsomes. Endocrinology, 134(3), 1401–1408. doi:10.1210/endo.134.3.8119180
[14] Betancor-Hernández, E., Pérez-Machı́n, R., Henrı́quez-Hernández, L., Mateos-Dı́az, C., Novoa-Mogollón, J., & Fernández-Pérez, L. (2003). Photoaffinity labeling identification of thyroid hormone-regulated glucocorticoid-binding peptides in rat liver endoplasmic reticulum: an oligomeric protein with high affinity for 16β-hydroxylated stanozolol. The Journal of Steroid Biochemistry and Molecular Biology, 87(4-5), 253–264. doi:10.1016/j.jsbmb.2003.09.009
[15] Bond P, Llewellyn W, Van Mol P. Anabolic androgenic steroid-induced hepatotoxicity. Med Hypotheses. 2016 Aug;93:150-3. doi: 10.1016/j.mehy.2016.06.004
[16] Sloane, D. E., Lee, C. W., & Sheffer, A. L. (2007). Hereditary angioedema: Safety of long-term stanozolol therapy. Journal of Allergy and Clinical Immunology, 120(3), 654–658. doi:10.1016/j.jaci.2007.06.037
[17] P. Niravath, Aromatase inhibitor-induced arthralgia: a review, Annals of Oncology, Volume 24, Issue 6, 2013, Pages 1443-1449, ISSN 0923-7534, doi.org/10.1093/annonc/mdt037.
